ЛАБОРАТОРНІ та ПРАКТИЧНІ РОБОТИ » Л.д.1-3 (2)
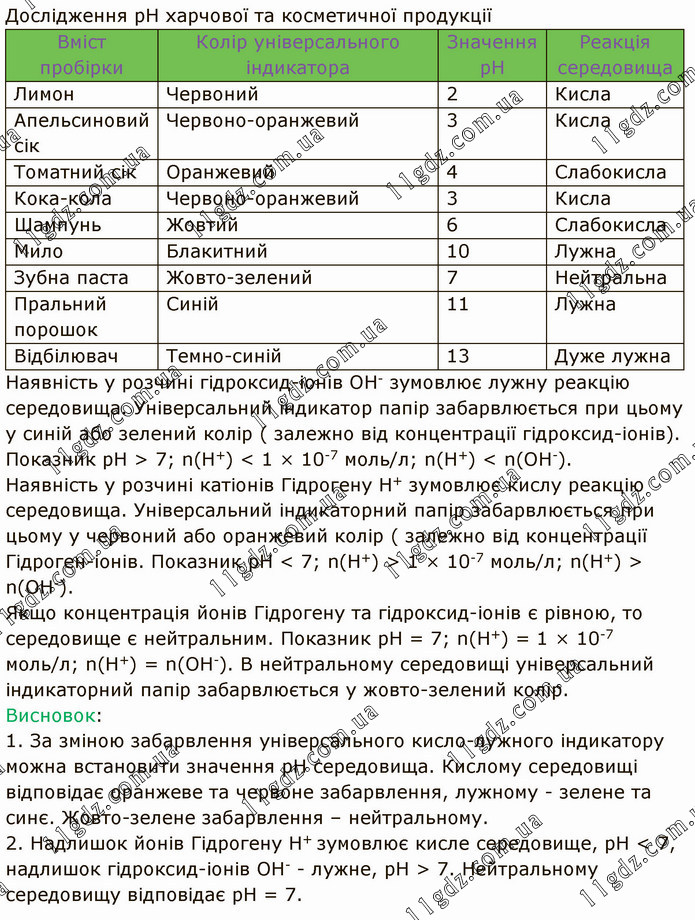
Дослідження рН харчової та косметичної продукції Наявність у розчині гідроксид-іонів ОН- зумовлює лужну реакцію середовища. Універсальний індикатор папір забарвлюється при цьому у синій або зелений колір ( залежно від концентрації гідроксид-іонів). Показник рН > 7; n(H+) < 1 × 10-7 моль/л; n(H+) < n(OH-). Наявність у розчині катіонів Гідрогену Н+ зумовлює кислу реакцію середовища. Універсальний індикаторний папір забарвлюється при цьому у червоний або оранжевий колір ( залежно від концентрації Гідроген-іонів. Показник рН < 7; n(H+) > 1 × 10-7 моль/л; n(H+) > n(OH-). Якщо концентрація йонів Гідрогену та гідроксид-іонів є рівною, то середовище є нейтральним. Показник рН = 7; n(H+) = 1 × 10-7 моль/л; n(H+) = n(OH-). В нейтральному середовищі універсальний індикаторний папір забарвлюється у жовто-зелений колір. Висновок: 1. За зміною забарвлення універсального кисло-лужного індикатору можна встановити значення рН середовища. Кислому середовищі відповідає оранжеве та червоне забарвлення, лужному - зелене та синє. Жовто-зелене забарвлення – нейтральному. 2. Надлишок йонів Гідрогену Н+ зумовлює кисле середовище, рН < 7, надлишок гідроксид-іонів ОН- - лужне, рН > 7. Нейтральному середовищу відповідає рН = 7.