Тема 3. ДОСЛІДЖУЄМО БУДОВУ АТОМА » Стр.147 (2)
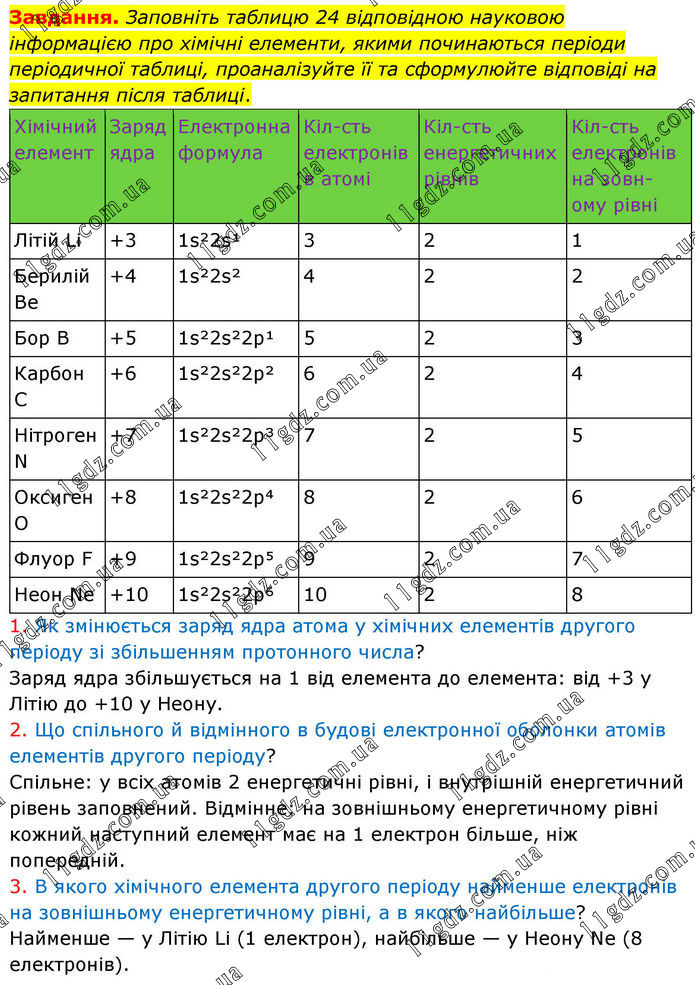
Завдання. Заповніть таблицю 24 відповідною науковою інформацією про хімічні елементи, якими починаються періоди періодичної таблиці, проаналізуйте її та сформулюйте відповіді на запитання після таблиці. 1. Як змінюється заряд ядра атома у хімічних елементів другого періоду зі збільшенням протонного числа? Заряд ядра збільшується на 1 від елемента до елемента: від +3 у Літію до +10 у Неону. 2. Що спільного й відмінного в будові електронної оболонки атомів елементів другого періоду? Спільне: у всіх атомів 2 енергетичні рівні, і внутрішній енергетичний рівень заповнений. Відмінне: на зовнішньому енергетичному рівні кожний наступний елемент має на 1 електрон більше, ніж попередній. 3. В якого хімічного елемента другого періоду найменше електронів на зовнішньому енергетичному рівні, а в якого найбільше? Найменше — у Літію Li (1 електрон), найбільше — у Неону Ne (8 електронів).