ТЕМА 1. Будова атома. Періодичний закон » §15 Впр.4(а)
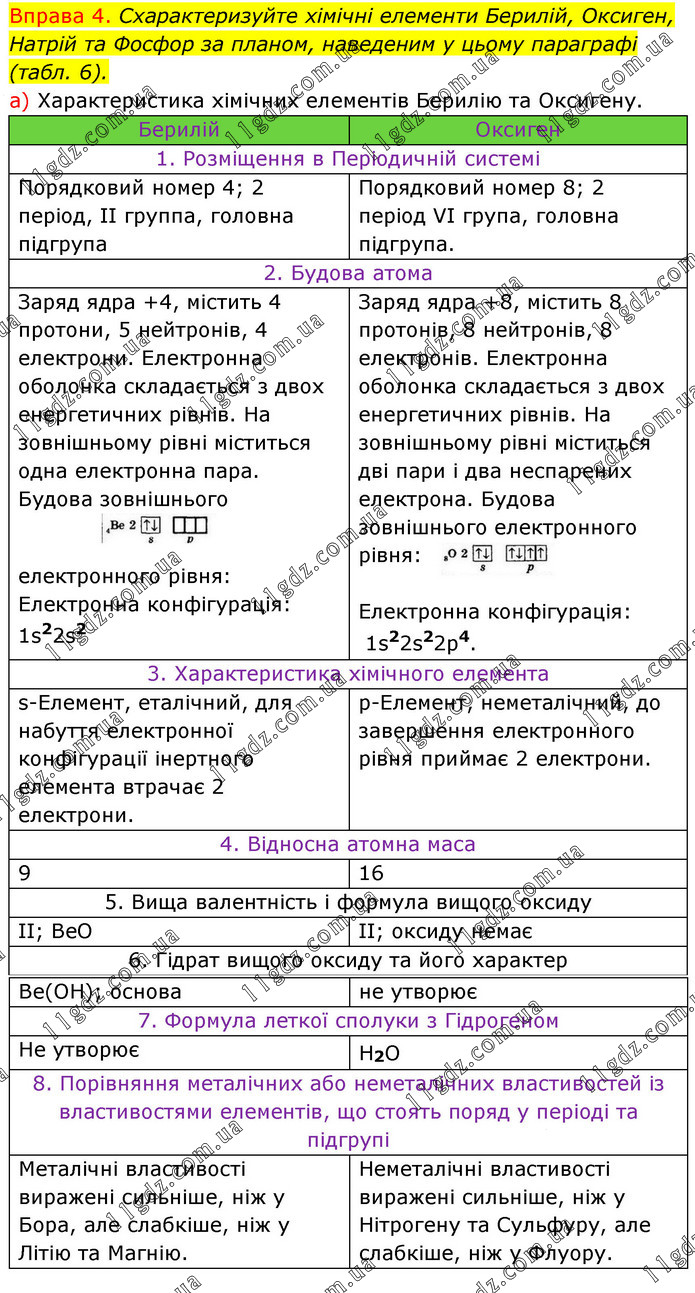
Вправа 4. Схарактеризуйте хімічні елементи Берилій, Оксиген, Натрій та Фосфор за планом, наведеним у цьому параграфі (табл. 6). а) Характеристика хімічних елементів Берилію та Оксигену. Берилій Оксиген 1. Розміщення в Періодичній системі Порядковий номер 4; 2 період, ІІ группа, головна підгрупа Порядковий номер 8; 2 період VI група, головна підгрупа. 2. Будова атома Заряд ядра +4, містить 4 протони, 5 нейтронів, 4 електрони. Електронна оболонка складається з двох енергетичних рівнів. На зовнішньому рівні міститься одна електронна пара. Будова зовнішнього електронного рівня: Електронна конфігурація: 1s22s2 Заряд ядра +8, містить 8 протонів, 8 нейтронів, 8 електронів. Електронна оболонка складається з двох енергетичних рівнів. На зовнішньому рівні міститься дві пари і два неспарених електрона. Будова зовнішнього електронного рівня: Електронна конфігурація: 1s22s22р4. 3. Характеристика хімічного елемента s-Елемент, еталічний, для набуття електронної конфігурації інертного елемента втрачає 2 електрони. р-Елемент, неметалічний, до завершення електронного рівня приймає 2 електрони. 4. Відносна атомна маса 9 16 5. Вища валентність і формула вищого оксиду ІІ; ВеО ІІ; оксиду немає 6. Гідрат вищого оксиду та його характер Ве(ОН); основа не утворює 7. Формула леткої сполуки з Гідрогеном Не утворює Н2О 8. Порівняння металічних або неметалічних властивостей із властивостями елементів, що стоять поряд у періоді та підгрупі Металічні властивості виражені сильніше, ніж у Бора, але слабкіше, ніж у Літію та Магнію. Неметалічні властивості виражені сильніше, ніж у Нітрогену та Сульфуру, але слабкіше, ніж у Флуору.